Equipo 4 biotransformacion de toxones
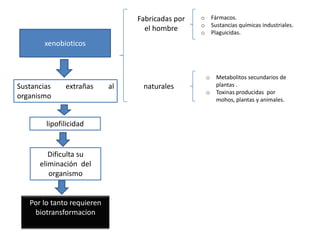
- 2. Fabricadas por o Fármacos. o Sustancias químicas industriales. el hombre o Plaguicidas. xenobioticos o Metabolitos secundarios de Sustancias extrañas al naturales plantas . o Toxinas producidas por organismo mohos, plantas y animales. lipofilicidad Dificulta su eliminación del organismo Por lo tanto requieren biotransformacion
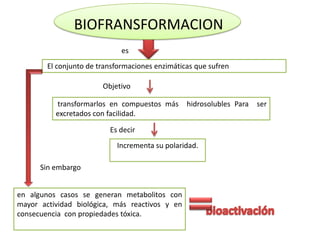
- 3. BIOFRANSFORMACION es El conjunto de transformaciones enzimáticas que sufren Objetivo transformarlos en compuestos más hidrosolubles Para ser excretados con facilidad. Es decir Incrementa su polaridad. Sin embargo en algunos casos se generan metabolitos con mayor actividad biológica, más reactivos y en consecuencia con propiedades tóxica.
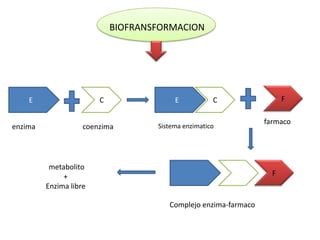
- 4. BIOFRANSFORMACION E C E C F farmaco enzima coenzima Sistema enzimatico metabolito + F Enzima libre Complejo enzima-farmaco
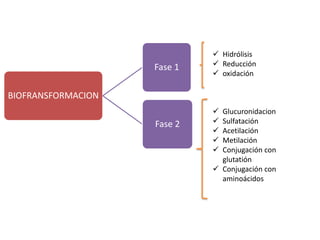
- 6. Hidrólisis Fase 1 Reducción oxidación BIOFRANSFORMACION Glucuronidacion Fase 2 Sulfatación Acetilación Metilación Conjugación con glutatión Conjugación con aminoácidos
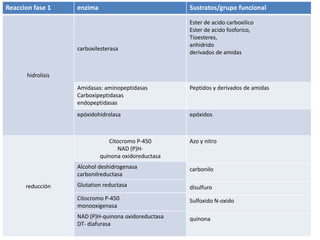
- 7. Reaccion fase 1 enzima Sustratos/grupo funcional Ester de acido carboxilico Ester de acido fosforico, Tioesteres, anhidrido carboxilesterasa derivados de amidas hidrolisis Amidasas: aminopeptidasas Peptidos y derivados de amidas Carboxipeptidasas endopeptidasas epóxidohidrolasa epóxidos Citocromo P-450 Azo y nitro NAD (P)H- quinona oxidoreductasa Alcohol deshidrogenasa carbonilo carbonilreductasa reducción Glutation reductasa disulfuro Citocromo P-450 Sulfoxido N-oxido monooxigenasa NAD (P)H-quinona oxidoreductasa quinona DT- diafurasa
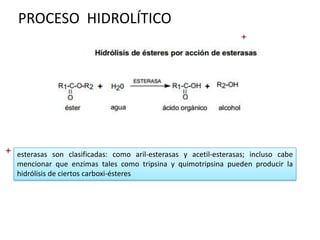
- 8. PROCESO HIDROLÍTICO esterasas son clasificadas: como aril-esterasas y acetil-esterasas; incluso cabe mencionar que enzimas tales como tripsina y quimotripsina pueden producir la hidrólisis de ciertos carboxi-ésteres
- 9. La hidrólisis de amidas es catalizada por amidasas; sin embargo, este proceso hidrolítico es más lento en comparación al proceso de hidrólisis de los ésteres. Adicionalmente, el plasma no es un lugar de alta actividad de hidrólisis de amidas, sino que ésta se presenta en otros tejidos, como es el caso de algunas carboxil-amidasas microsomales del hígado
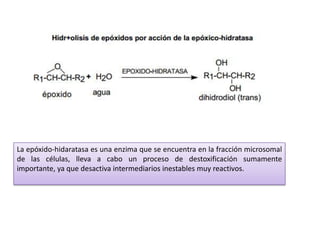
- 10. La epóxido-hidaratasa es una enzima que se encuentra en la fracción microsomal de las células, lleva a cabo un proceso de destoxificación sumamente importante, ya que desactiva intermediarios inestables muy reactivos.
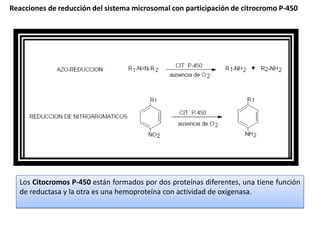
- 11. Reacciones de reducción del sistema microsomal con participación de citrocromo P-450 Los Citocromos P-450 están formados por dos proteínas diferentes, una tiene función de reductasa y la otra es una hemoproteína con actividad de oxigenasa.
- 12. OXIDACIÓN
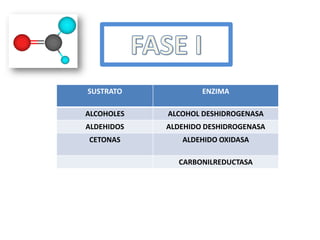
- 13. SUSTRATO ENZIMA ALCOHOLES ALCOHOL DESHIDROGENASA ALDEHIDOS ALDEHIDO DESHIDROGENASA CETONAS ALDEHIDO OXIDASA CARBONILREDUCTASA
- 16. ENZIMAS: Alcohol deshidrogenasa. SUSTRATOS: Aldehído deshidrogenasa. Alcoholes. Aldehído oxidasa. Aldehídos. Carbonilreductasa. Cetonas La alcohol deshidrogenasa es una enzima citosólica que contiene cinc, presente en el tejido adiposo, así como en menor proporción, en el riñón, los pulmones y la mucosa gástrica. La alcohol deshidrogenasa presenta varias isozimas con distinta capacidad para oxidar el etanol.
- 17. La deshidrogenasa gástrica presenta menor afinidad con el etanol que la hepática, a pesar de lo cual el metabolismo gástrico del alcohol puede revestir gran importancia especialmente cuando se ingiere grandes cantidades de este compuesto. Posee menor actividad en las mujeres que en los hombres
- 18. La oxidación del alcohol a aldehído se produce en oCitocromo p-450 los microsomas y peroxisomas . o Catalasa. La oxidación de aldehídos a ácidos tiene lugar por acción de la aldehído deshidrogenasa
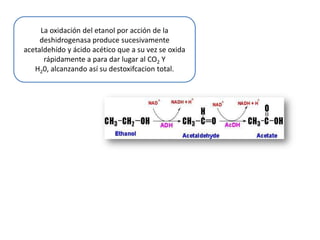
- 19. La oxidación del etanol por acción de la deshidrogenasa produce sucesivamente acetaldehído y ácido acético que a su vez se oxida rápidamente a para dar lugar al CO2 Y H20, alcanzando así su destoxifcacion total.
- 20. REACCIONES DE FASE ll
- 21. Conjugación con acido glucorónico La formación de conjugados con el acido glucorónico es una vía fundamental de biotransformacion en todos los mamíferos , con excepción de los felinos. Grupos funcionales de El cofactor de esta Sistema enzimático los sustratos de la conjugación implicado conjugación • Acido uridina-difosfato • UDP-glucuronosil • Los alcoholes alifáticos y glucurónico (acido transferasa . fenoles que forman los UDP-glucurónico). • Ubicada en el retículo éteres. endoplásmico, sobre • Los ácidos carboxílicos todo de las células que forman esteres. hepáticas, aunque • Las aminas primarias y también del riñón piel secundarias (alifáticas y y mucosa aromáticas) gastrointestinal • Moléculas poseedoras de grupos sulfhidrilo
- 22. Se aplica: La vía de conjugación con •Los xenobióticos acido glucurónico •Los compuestos endógenos: bilirrubina, los esteroides y las hormonas tiroideas Los conjugados con ácido glucurónico son moléculas polares , Fácilmente excretables por la hidrosolubles. orina o la bilis dependiendo del peso molecular del compuesto original o su metabolito de fase I.
- 23. La solubilidad en agua que le confiere La presencia en el conjugado del grupo acido fuerte del acido glucurónico, ionizado en las condiciones de pH fisiológico favorece la eliminación tanto por: Ser un grupo reconocido como sustrato aniónico por los sistemas de transporte activo de la excreción biliar y renal.
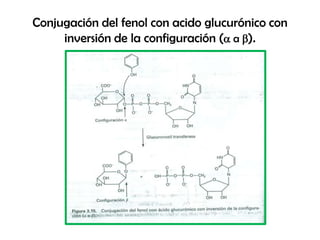
- 24. Conjugación del fenol con acido glucurónico con inversión de la configuración (a a b).
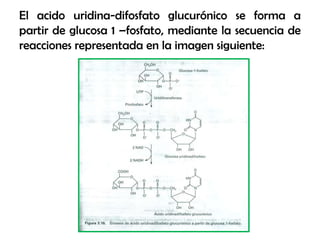
- 25. El acido uridina-difosfato glucurónico se forma a partir de glucosa 1 –fosfato, mediante la secuencia de reacciones representada en la imagen siguiente:
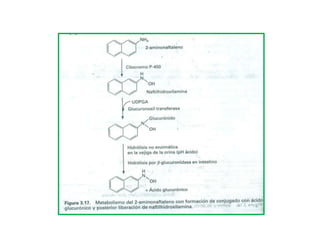
- 26. La conjugación con ácido glucuronico Este es el caso de ciertas es una vía importante de aminas aromáticas, como el desintoxicación. 2-aminonaftaleno, un agente cancerígeno de la vejiga urinaria. En ciertos casos puede potenciar la El mecanismo de toxicidad toxicidad de xenobióticos. consiste en la oxidación hepática del compuesto original , con formación de hidroxilamina. Este metabolito se conjuga a continuación con acido glucurónico y el conjugado se excreta a través de la orina.
- 28. Conjugación con sulfatos o sulfonación La conjugación con sulfato es una vía importante de transformación de los xenobióticos y los compuestos endógenos que contienen los grupos funcionales alcohol y amino. Compuestos que se La reacción El cofactor de la conjugan conjugación • Alcoholes alifáticos y • Tiene lugar por • 3’-fosfoadenosina-5’- aromáticos. catálisis de enzimas fosfosulfato (PAPS) • Aminas e solubles: las del que se transfiere el hidroxilaminas, sulfotranferasas. grupo sulfato. • Las aminas alifáticas e • Presentes en el citosol hidroxiamidas de las células del aromáticas, como el hígado, los riñones, la N-hidroxi-2- mucosa acetilaminofluoreno. gastrointestinal, los pulmones, las plaquetas y el cerebro.
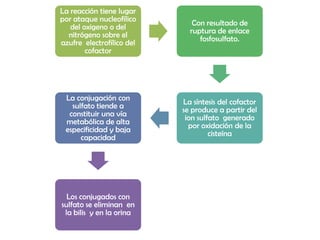
- 29. La reacción tiene lugar por ataque nucleofílico Con resultado de del oxigeno o del ruptura de enlace nitrógeno sobre el fosfosulfato. azufre electrofílico del cofactor La conjugación con La síntesis del cofactor sulfato tiende a se produce a partir del constituir una vía ion sulfato generado metabólica de alta por oxidación de la especificidad y baja cisteína capacidad Los conjugados con sulfato se eliminan en la bilis y en la orina
- 30. • La conjugación con sulfatos es normalmente un proceso de destoxificación, si bien en algunos casos pueden formarse sulfatos inestables que finalmente se descomponen con formación de especies electrofílicas altamente toxicas. Por ejemplo: la acción cancerígena del 2-acetilaminofluoreno se atribuye a la formación de sendas especies como consecuencia de la descomposición de los respectivos conjugados sulfonado.
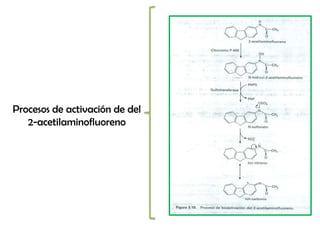
- 31. Procesos de activación de del 2-acetilaminofluoreno
- 32. La activación del 2-acetilaminofluoreno tiene lugar por sulfonación del metabolito hidroxilado por el citocromo P-450, que por perdida del ion sulfato produce iones nitrenio y carbonio, responsables directos de los efectos cancerígenos de este compuesto.
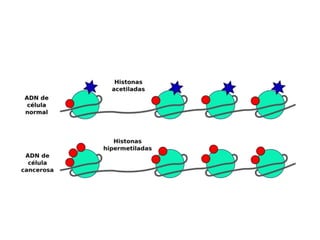
- 33. Modificación de Histonas o Metilación del ADN Acetilación • a lo largo del ADN existen • las histonas son proteínas en dinucleótidos CpG, unión de las cuales el ADN se enrolla citosina con guanina. dando origen a una estructura • Estos dinucleótidos se llamada nucleosoma. encuentran en mayor • Los aminoácidos de las medida en las regiones histonas sufren modificaciones promotoras de genes (islas por acetilación, metilación y CpG), zonas de inicio de la fosforilación mediante ciertas transcripción génica enzimas.
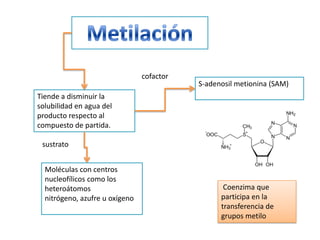
- 34. cofactor S-adenosil metionina (SAM) Tiende a disminuir la solubilidad en agua del producto respecto al compuesto de partida. sustrato Moléculas con centros nucleofílicos como los heteroátomos Coenzima que nitrógeno, azufre u oxígeno participa en la transferencia de grupos metilo
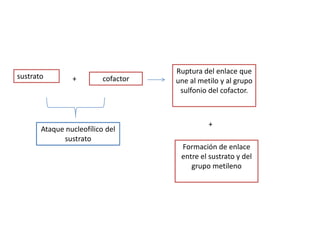
- 35. Ruptura del enlace que sustrato + cofactor une al metilo y al grupo sulfonio del cofactor. + Ataque nucleofílico del sustrato Formación de enlace entre el sustrato y del grupo metileno
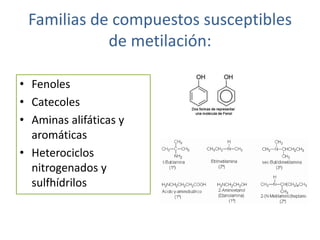
- 36. Familias de compuestos susceptibles de metilación: • Fenoles • Catecoles • Aminas alifáticas y aromáticas • Heterociclos nitrogenados y sulfhídrilos
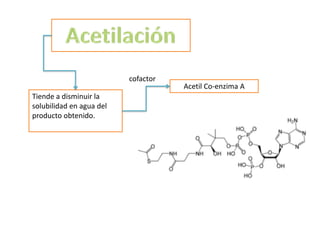
- 37. cofactor Acetil Co-enzima A Tiende a disminuir la solubilidad en agua del producto obtenido.
- 38. Existen dos categorías: Acetiladores Acetiladores rápidos lentos Son mas susceptibles a la toxicidad de los xenobióticos cuya Poseen varias biotransformación tiene modificaciones en uno lugar por este mecanismo. de los dos genes que modifican las N-acetil transferasas, que provoca un descenso en la actividad y estabilidad de dichas enzimas.
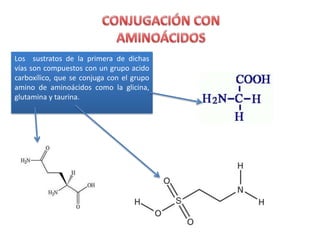
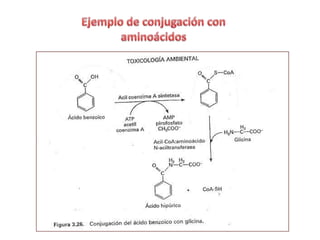
- 40. Los sustratos de la primera de dichas vías son compuestos con un grupo acido carboxílico, que se conjuga con el grupo amino de aminoácidos como la glicina, glutamina y taurina.
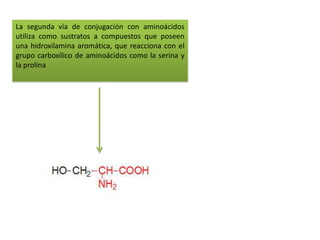
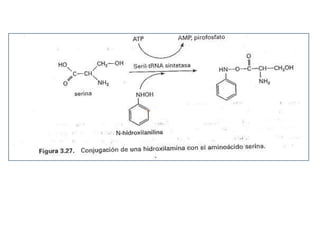
- 42. La segunda vía de conjugación con aminoácidos utiliza como sustratos a compuestos que poseen una hidroxilamina aromática, que reacciona con el grupo carboxílico de aminoácidos como la serina y la prolina
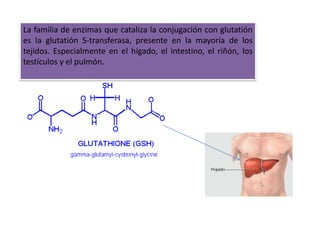
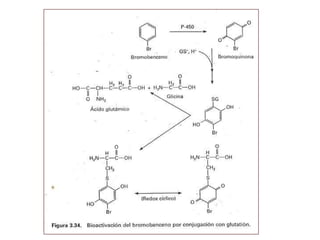
- 44. El glutatión es un tripeptido formado por glicina, cisteína y acido glutamico. Los sustratos para la conjugación con glutatión son compuestos electrofilicos o sus precursores, capaces de convertirse en especies electrofilicas como resultado de reacciones de biotransformacion.
- 45. La familia de enzimas que cataliza la conjugación con glutatión es la glutatión S-transferasa, presente en la mayoría de los tejidos. Especialmente en el hígado, el intestino, el riñón, los testículos y el pulmón.
- 46. Las reacciones de sustitución: ocurren preferentemente cuando el sustrato posee un buen grupo saliente, como los halógenos , sulfatos , sulfonatos, fosfatos o el grupo nitro, unido aun átomo de carbono alilico o bencílico. Las reacciones de adición de glutatión a un doble en lace carbono-carbono, también se ven favorecidas por la presencia en la molécula del sustrato de grupos retiradores de electrones.
- 47. Es un proceso de enorme importancia desde el punto de vista toxicológico, ya que sus sustratos son especies electrofilicas capaces de reacciones de gran trascendencia bioquímica, como el ataque a centros nucleofílicos del ADN y de las proteínas celulares. Aunque los efectos de la conjugación con glutatión son en la gran mayoría de los casos beneficiosos desde el punto de vista de la destoxificacion, en ciertas ocasiones se pueden producir metabolitos activos, mas tóxicos que los compuesto de partida.